 |
مبدأ عمل الخلية الغلفانية
مثال:
تمثل المعادلة التالية التفاعل الذي يحدث في خلية غلفانية قطباها (نيكل - نحاس):
Ni (s) + Cu2+ (aq) → Ni2+ (aq) + Cu (s)
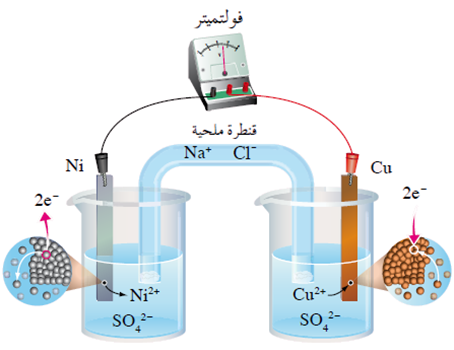
تتكون الخلية من وعائين:
الوعاء الأول: يحتوي على قطب نيكل مغموس في محلول كبريتات النيكل NiSO4، ويُسمى نصف خلية نيكل.
الوعاء الثاني: يحتوي على قطب نحاس مغموس في محلول كبريتات النحاس CuSO4، ويُسمى نصف خلية نحاس.
يتصل القطبان معاً بأسلاك فلزية موصولة بفولتميتر.
يتصل المحلولان معاً بقنطرة ملحية.
ماذا يحدث في نصف خلية النيكل؟
يلاحظ من المعادلة أن النيكل قد تأكسد، لذا فهو يمثل المصعد في هذه الخلية، وإشارة قطبه سالبة، ويتأكسد القطب كما في المعادلة:
نصف تفاعل التأكسد/المصعد Ni (s) → Ni2+ (aq) + 2e-
تتجه الإلكترونات الناتجة من تأكسد القطب عبر الأسلاك مروراً بالفولتميتر فينحرف المؤشر نحو قطب النحاس.
بفعل تأكسد النيكل يتحول إلى أيونات Ni2+ فتقل كتلة القطب، وتزداد تركيز أيونات Ni2+ ، فيصبح تركيزها أعلى من تركيز الأيونات السالبة في المحلول.
ماذا يحدث في نصف خلية النحاس؟
يلاحظ من المعادلة أن أيونات النحاس قد اختزلت، لذا فقطب النحاس يمثل المهبط في هذه الخلية، وإشارة قطبه موجبة، وتُختزل أيونات النحاس بفعل الإلكترونات القادمة من قطب النيكل كما في المعادلة:
نصف تفاعل الاختزال/المهبط Cu2+ (aq) + 2e- → Cu (s)
بفعل اختزال أيونات النحاس Cu2+ تتحول إلى ذرات نحاس تتجمع على قطب النحاس، فتزداد كتلة القطب، ويقل تركيز أيونات Cu2+ ، فيصبح تركيزها أقل من تركيز الأيونات السالبة في المحلول.
ويأتي دور القنطرة الملحية فتعمل على حفظ التوازن الكهربائي، عن طريق موازنة الشحنات الكهربائية في الخلية أثناء عملها.
والآن املأ الجدول التالي فيما يتعلق بالخلية الغلفانية:
|
وجه المقارنة |
المصعد |
المهبط |
|
شحنة القطب (إشارته) |
|
|
|
العملية التي تحدث عليه |
|
|
|
كتلة القطب |
|
|
|
تركيز أيوناته الموجبة |
|
|
|
حركة الإلكترونات |
|
|
|
اتجاه مؤشر الفولتميتر |
|
|
|
معادلة نصف التفاعل العامة |
|
|
سؤال 1 :
تمثل المعادلة التالية التفاعل الذي يحدث في خلية غلفانية قطباها من الكادميوم والقصدير:
Sn2+(aq) + Cd(s) → Sn(s) + Cd2+(aq)
- أي القطبين يمثل المصعد، وأيهما يمثل المهبط، وما شحنة كل منهما؟
- اكتب معادلة نصف التفاعل الذي يحدث عند كل قطب.
- وضح اتجاه حركة الإلكترونات في الدارة الخارجية.
- إلى أي الأقطاب يتحرك مؤشر الفولتميتر؟
- أي القطبين ستنقص كتلته؟
- ماذا يحدث لتركيز أيونات Cd2+ ؟
الحل:
- بما أن عملية التأكسد قد حدثت على قطب الكادميوم Cd لذا فهو يمثل المصعد وإشارته سالبة، وبما أن عملية الاختزال قد حدثت على قطب القصدير Sn لذا فهو يمثل المهبط وإشارته موجبة.
- نصف تفاعل التأكسد/المصعد: → Cd2+ + 2e- Cd
نصف تفاعل الاختزال/المهبط: Sn2+ + 2e- → Sn
- تتحرك الإلكترونات في الدارة الخارجية من قطب الكادميوم (المصعد) إلى قطب القصدير (المهبط).
- يتحرك مؤشر الفولتميتر نحو قطب القصدير (المهبط).
- قطب الكادميوم.
- تزداد.
سؤال 2 :
تمثل المعادلة التالية التفاعل الذي يحدث في خلية (خارصين - فضه):
Zn (s) + 2Ag+(aq) → Zn2+ (aq) + 2Ag (s)
- أي القطبين يمثل المصعد وأيهما يمثل المهبط، وما شحنة كل منهما؟
- اكتب معادلة نصف التفاعل الذي يحدث عند كل قطب.
- وضح اتجاه حركة الإلكترونات في الدارة الخارجية واتجاه مؤشر الفولتميتر.
- أي القطبين تقل كتلته؟
- ماذا يحدث لتركيز أيونات Ag+ ؟
سؤال 3 :
الشكل التالي يمثل خلية غلفانية، استعن بالشكل للإجابة عن الأسئلة التالية:
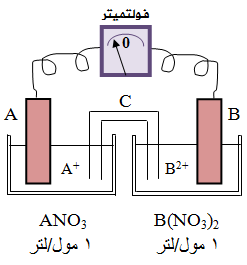
- أي القطبين يمثل المصعد؟ وما شحنته؟
- اكتب معادلة نصف التفاعل الذي يحدث عند كل قطب.
- اكتب المعادلة الموزونة للتفاعل الكلي.
- ماذا يحدث لكتلة صفيحة B مع مرور الزمن؟
- ما الذي يمثله الرمز (C) في الخلية، وما دورها؟
- ما تحولات الطاقة في هذه الخلية؟
سؤال 4 :
في خلية غلفانية قطباها من الفلزين (M/Q) ينحرف مؤشر الفولتميتر باتجاه قطب M ، إذا علمت أن M أيون ثنائي الشحنة في مركباته، و Q أيون ثلاثي الشحنة في مركباته، أجب عما يلي:
- حدّد المصعد في الخلية.
- أي القطبين تزداد كتلته.
- ما شحنة قطب M ؟
- في أي وعائي الخليتين يزداد تركيز الأيون الموجب؟
- اكتب معادلة موزونة تمثّل التفاعل الكلي الذي يحدث في الخلية.
سؤال 5 : أسئلة وزارية موضوعية
1- إذا كان التفاعل الآتي يحدث في إحدى الخلايا الغلفانية: Mn(s) + Cd2+(aq) → Mn2+(aq) + Cd(s) فإن:
أ) القطب Cd هو القطب السالب.
ب) كتلة القطب Mn تزداد.
ج) الإلكترونات تسري من القطب Cd إلى القطب Mn
د) تركيز أيونات Mn2+ يزداد.
2- يكون المصعد في الخلية الغلفانية هو القطب:
أ) السالب الذي تحدث عنده عملية التأكسد.
ب) السالب الذي تحدث عنده عملية الاختزال.
ج) الموجب الذي تحدث عنده عملية التأكسد.
د) الموجب الذي تحدث عنده عملية الاختزال.
3- في الخلية الغلفانية يكون:
أ) المهبط سالب.
ب) الاختزال على المصعد.
ج) التفاعل تلقائي.
د) جهد الخلية سالب.
4- أي العبارات الآتية تتفق والخلية الغلفانية:
أ) Eº الخلية سالب.
ب) التفاعل تلقائي.
ج) يحدث الاختزال عند المصعد.
د) إشارة المهبط سالبة.
5- في الخلية الغلفانية يكون:
أ) التفاعل غير تلقائي.
ب) التأكسد على المهبط.
ج) المصعد سالب.
د) تتحول الطاقة من كهربائية إلى كيميائية.