 |
إجابات أسئلة مراجعة الدرس الثاني
الذائبية
السؤال الأول:
الفكرة الرئيسة: أذكر العوامل التي تعتمد عليها كمية المادة التي تذوب في كمية محددة من الماء.
تعتمد كمية المادة التي تذوب في كمية محددة من الماء على طبيعة المادة، ودرجة الحرارة.
السؤال الثاني:
أكمل الفراغ في ما يأتي بالمفهوم العلمي المناسب:
1) أكبر كمية من المذاب تذوب في (100g) من الماء عند درجة حرارة معينة تُسمى الذائبية.
2) تُعرف عملية استخلاص الأملاح من محاليلها للحصول على الماء والملح بـ التقطير.
3) المادة التي تفكك جسيمات المذاب في المحلول، تُسمى المذيب.
السؤال الثالث:
أفسر كيف يمكن الحصول على ماء نقي من محلول السكر في الماء؟
يمكن الحصول على السكر من المحلول بتبخير الماء كاملاً ثم تكثيفه، أو التقطير.
السؤال الرابع:
أقارن بين تأثير درجة الحرارة في ذائبية كل من: المواد الصلبة والغازات في الماء.
تزداد ذائبية المواد الصلبة بزيادة درجة الحرارة، بينما تقل ذائبية الغازات بزيادة درجة الحرارة.
السؤال الخامس:
أَستخدم الأرقام: أحسب كتلة ملح كبريتات النحاس بالغرامات اللازم إضافتها إلى 50 mL من محلول تركيزه 0.4 g/mL .
C =
0.4 g/mL =
m = 20 g
السؤال السادس:
التفكير الناقد: كيف يمكنني التأكد أن المذاب ما زال موجوداً في المحلول من دون أن أتذوقه؟
عند تسخين المحلول، تقل ذائبية الملح، فيتبخر المذيب ويترسب المذاب.
تطبيق الرياضيات
1- أَستخدم الأرقام: أذيب (30g) من الملح في كمية كافية من الماء، فأصبح حجم المحلول (300 mL)، أحسب تركيزه.
C =
V = = 0.1 g/mL
2- 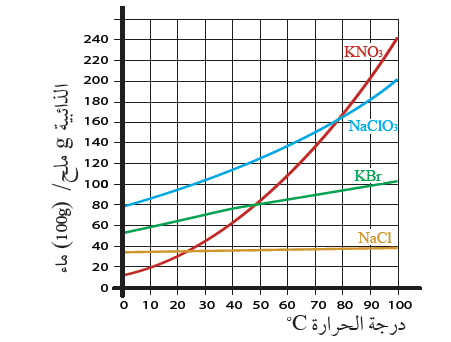 أدرس الشكل المجاور، ثم أجيب عن الأسئلة الآتية:
أدرس الشكل المجاور، ثم أجيب عن الأسئلة الآتية:
1- ما العامل الذي يؤثر في ذائبية الأملاح؟
درجة الحرارة.
2- ما ذائبية كل من: NaCl ، و KBr عند درجة حرارة 80oC ؟
ذائبية NaCl = (39 g)، ذائبية = (98 g).
3- أصف ما يحدث لملح نترات البوتاسيوم KNO3 عند تبريد المحلول من درجة حرارة 80oC إلى 40oC .
تقل ذائبية الملح بانخفاض درجة الحرارة، وتترسب كمية من الملح.