 |
الروابط الكيميائية وأنواعها
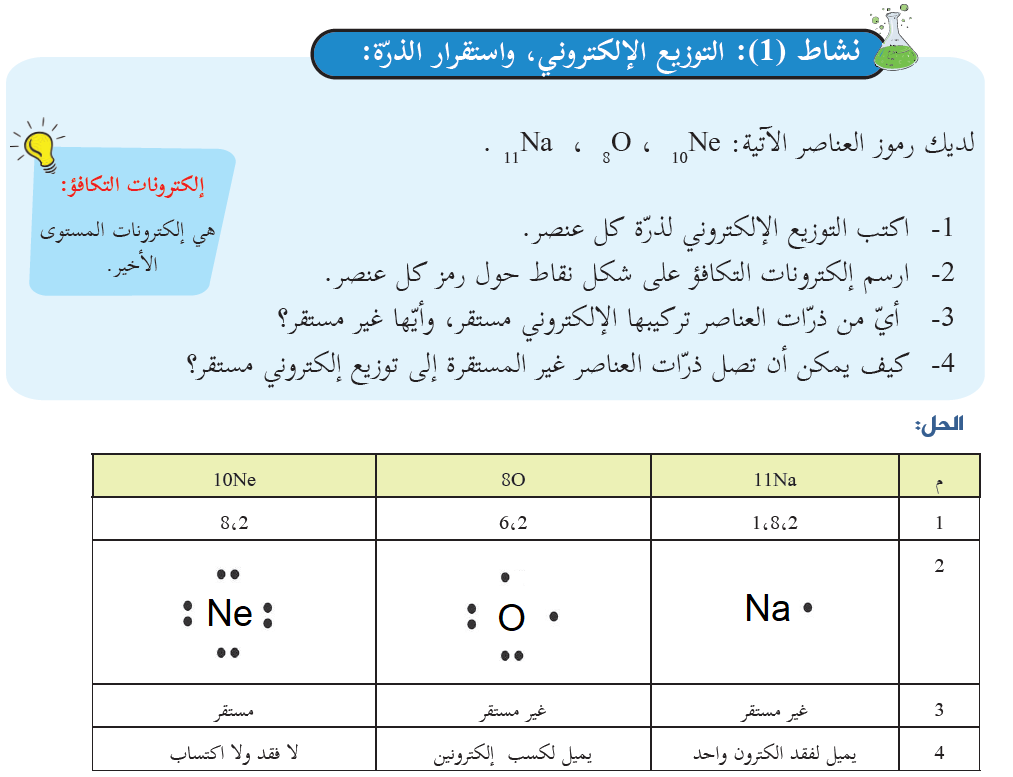
علاقة التوزيع الإلكتروني باستقرار الذرة
تميل الذرة للارتباط بغيرها للوصول إلى توزيع إلكتروني مشابه لأقرب غاز نبيل لها، وذلك عن طريق فقد الإكترونات كسبها أو المشاركة بها. وتحدد إلكترونات التكافؤ عدد الإلكترونات التي يتم فقدها أو كسبها أو المشاركة بها.
أنواع الروابط
- الروابط الأولية: وهي روابط كيميائية تنشأ بين الذرات أو الأيونات، وهي على ثلاثة أنواع:
- الروابط الأيونية.
- الروابط التساهمية.
- الروابط الفلزية.
- الروابط الثانوية: وهي قوى تجاذب ضعيفة تنشأ بين ذرات الغازات النبيلة، أو بين الجزيئات، وهي على ثلاثة أنواع:
- قوى التجاذب بين الجزيئات ثنائيات القطب.
- الروابط الهيدروجينية.
- قوى لندن.