ثانياً: تفاعلات الإحلال
تفاعل الإحلال: تفاعل يحل فيه عنصر نشط "أكثر فاعلية" محل عنصر آخر ذي نشاط أقل "أقل فاعلية" في مركب آخر.
ويُحَدَد العنصر الأكثر نشاطاً من خلال متسلسلة النشاط الكيميائي.
متسلسلة النشاط الكيميائي: ترتيب العناصر الفلزية تنازلياً حسب درجة نشاطها الكيميائي، ويحل العنصر الأكثر نشاطاً محل العنصر الأقل نشاطاً.
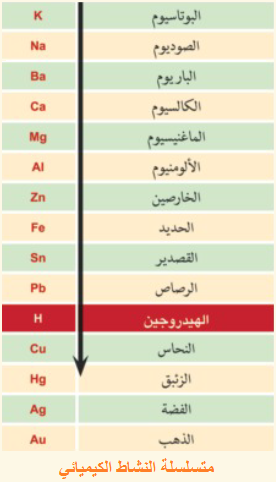
ومن خلال المتسلسلة يمكن ملاحظة ما يلي:
العناصر التي تقع في أعلى المتسلسلة تحل محل العناصر التي تقع في أسفل السلسلة.
مثال:
يحل البوتاسيوم محل الصوديوم في مركباته ولا يحل الصوديوم محل البوتاسيوم في مركباته.
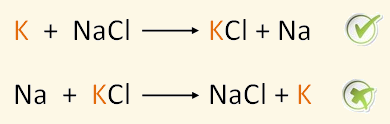
كما يمكن ملاحظة أن العناصر التي تسبق الهيدروجين في السلسلة تحل محل الهيدروجين في الأحماض، أما التي تلي الهيدروجين في السلسلة فلا تحل محله في الأحماض إلا بشروط كيميائية خاصة.
مثال:
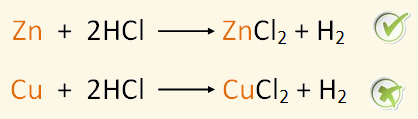
يحل الخارصين محل الهيدروجين عند تفاعله مع حامض الهيدروكلوريك، بينما لا يستطيع النحاس أن يحل محل الهيدروجين عند تفاعله مع حامض الهيدروكلوريك.
أنواع تفاعلات الإحلال
تقسم تفاعلات الإحلال إلى قسمين، هما:
- تفاعلات الإحلال البسيط.
- تفاعلات الإحلال المزدوج.
إعداد : شبكة منهاجي التعليمية
10 / 01 / 2023
النقاشات