أسئلة المحتوى وإجاباتها
نظرية تنافر أزواج إلكترونات مستوى التكافؤ
أتحقق صفحة (17):
أرسم تركيب لويس لكل من الجزيئات الآتية، وأحدد عدد أزواج الإلكترونات الرابطة وغير الرابطة في ذرتها المركزية:
OF2 , BeCl2
جزيء BeCl2 :
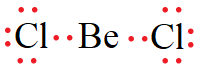
عدد أزواج الإلكترونات الرابطة = 2
عدد أزواج الإلكترونات غير الرابطة في الذرة المركزية = 0
جزيء OF2 :

عدد أزواج الإلكترونات الرابطة = 2
عدد أزواج الإلكترونات غير الرابطة في الذرة المركزية = 2
أستنتج صفحة (18):
أستنتج العلاقة بين عدد أزواج الإلكترونات حول الذرة المركزية ومقدار الزاوية بين الروابط في الجزي.
بزيادة عدد أزواج الإلكترونات الرابطة حول الذرة المركزية تقل الزاوية بين الروابط.
أفكر صفحة (21):
يحقق الأكسجين في مركباته قاعدة الثمانية، فما الشكل المتوقع لجزيء الأوزون O3 ، وكيف تترتب أزواج الإلكترونات حول الذرة المركزية؟
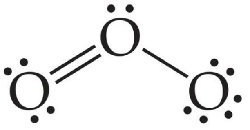
أتحقق صفحة (22):
أقارن بين الجزيئات الآتية من حيث الشكل الفراغي ومقدار الزاوية بين الروابط:
C2H2 , BF3 , BeH2
|
الجزيء |
الشكل الفراغي |
مقدار الزاوية بين الروابط |
|
BeH2 |
خطي |
180o |
|
BF3 |
مثلث مستوٍ |
120o |
|
C2H2 |
خطي |
180o |
إعداد : شبكة منهاجي التعليمية
03 / 07 / 2024
النقاشات