أسئلة إضافية
السؤال الأول:
ضع دائرة حول رمز الإجابة الصحيحة في الفقرات الآتية:
- قوى ثنائية القطب تربط بين:
أ- الجزيئات غير القطبية.
ب- الجزيئات القطبية.
ج- المركبات الأيونية.
د- الفلزات.
- المركب الذي تترابط جزيئاته بأعلى قوى تجاذب هو:
أ- C2H6
ب- C4H10
ج- CH4
د- C3H8
- المركب الذي تتماسك جزيئاته بقوى لندن فقط هو:
أ- CH3Cl
ب- CH3OH
ج- CCl4
د- CH3NH2
- إحدى المواد التالية ترتبط جزيئاتها بشكل رئيس بقوى لندن وهي:
أ- H2S
ب- CH3F
ج- CH3Cl
د- CO2
- ترتيب الجزيئات ( HCl , H2O , CH4 , HBr ) حسب تناقص قوى الترابط بين جزيئاتها في الحالة السائلة هو:
أ- CH4 < H2O < HCl < HBr
ب- HCl < HBr < H2O < CH4
ج- CH4 < HCl < H2O < HBr
د- CH4 < HCl < HBr < H2O
- المادة التي تترابط وحداتها البنائية الأساسية في الحالة السائلة بقوى لندن فقط هي:
أ- CHCl3
ب- Ar
ج- PF3
د- NH3
- أحد المواد الآتية ترتبط ذراتها بقوى لندن وهي:
أ- N2
ب- Na
ج- Ne
د- CO2
- المادة (في الحالة السائلة) التي ترتبط جزيئاتها بأضعف قوى ترابط هي:
أ- CH3CH2OH
ب- (C2H5)2O
ج- CH3CH2CH2CH3
د- CH3COCH3
السؤال الثاني:
صنف المواد الآتية حسب نوع قوى الترابط بين جزيئاتها في الحالة السائلة، كما هو مبين في الجدول:
CH3CH2CH2CH2OH , O2 , CH3CH2NH2 , N2 , CH3F , H2S , OF2 , Kr , Br2 , CH3CH2CH3 , HBr, ICl , SiCl4 , NO
|
مواد ترتبط دقائقها بقوى لندن فقط |
مواد ترتبط دقائقها بقوى تجاذب هيدروجيني |
مواد ترتبط دقائقها بقوى تجاذب ثنائيات القطب |
|
CH4 |
HF |
HCl |
|
|
|
|
|
|
|
|
السؤال الثالث:
أي المركبين HOCH2CH2OH و CH3CH2CH2OH تتوقع أن يكون له درجة غليان أعلى؟ فسّر إجابتك.
السؤال الرابع:
أي المركبين CH3CH2CH2CH2NH2 و CH3CH2CH2NH2 تتوقع أن يكون له درجة غليان أعلى؟ فسّر إجابتك.
السؤال الخامس:
رتب المركبات التالية تصاعدياً حسب قوى التجاذب بين جزيئاتها:

السؤال السادس:
ما نوع قوى التجاذب الرئيسة بين جزيئات أو ذرات كلّ من المواد الآتية إذا كانت في الحالة السائلة:
I2 , H2S , Ar , NO , O2 , C3H7NH2 , C8H18 , C2H5OH
السؤال السابع:
فسر ما يأتي:
أ- الرابطة B-F قطبية، والجزيء BF3 غير قطبي.
ب- درجة غليان المركب HOCH2CH2OH أعلى من درجة غليان المركب CH3CH2CH2OH بالرغم من تقارب كتلتيهما المولية.
ج- الروابط بين جزيئات CH3F ليست روابط هيدروجينية.
السؤال الثامن:
رتب الجزيئات الآتية تبعاً لزيادة درجة غليانها:
CH3CH2CH2CH3
CH3CH2CH2NH2
CH3CH2CH2CH2NH2
(CH3)3CH
السؤال التاسع:
ادرس الشكل الذي يمثل درجات غليان مركبات الهيدروجين مع عناصر المجموعات: الرابعة، والخامسة، والسادسة، والسابعة من الجدول الدوري، ثم أجب عن الأسئلة التي تليه.
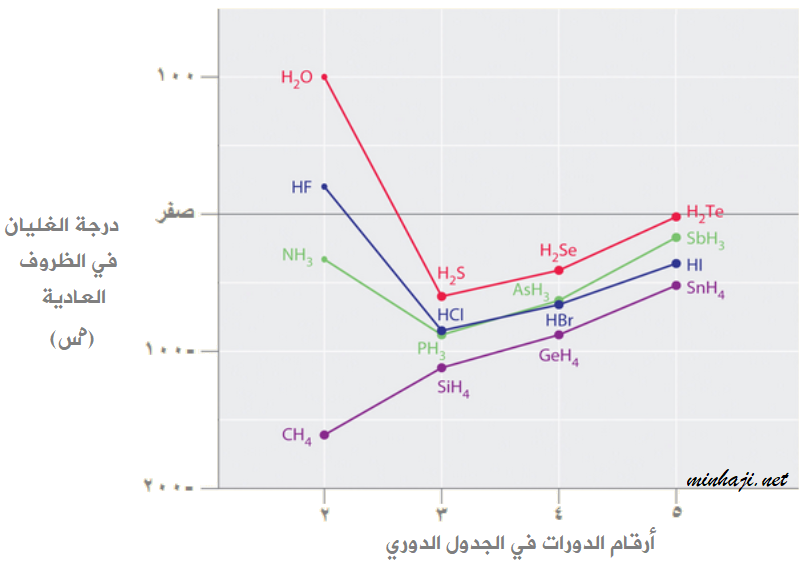
أ- كيف تتغير درجة الغليان بزيادة الكتلة المولية بشكلٍ عام.
ب- فسّر:
- ارتفاع درجة غليان الماء مقارنة بمركبات عناصر المجموعة السادسة.
- ارتفاع درجة غليان المركب HF مقارنة بمركبات عناصر المجموعة السابعة.
- نقصان درجة غليان المركب CH4 مقارنة بعناصر المجموعة الرابعة.
إعداد : شبكة منهاجي التعليمية
03 / 07 / 2024
النقاشات