بنية الذرة
تتركب الذرة من نواة موجبة الشحنة، تدور حولها إلكترونات سالبة الشحنة.
أولاً: النواة
- توجد النواة في مركز الذرة.
- تتركز كتلة الذرة في النواة.
تحتوي النواة على جسيمين، هما:
- البروتونات وهي جسيمات موجبة الشحنة.
- النيوترونات وهي جسيمات متعادلة الشحنة.
ثانياً: الإلكترونات
وهي جسميات سالبة الشحنة، وذات كتلة ضئيلة جداً، وتدور حول النواة بسرعة عالية في مناطق تسمى مستويات الطاقة.
العدد الذري والعدد الكتلي
لكل عنصر عدد ذري خاص، ويمثل العدد الذري عدد البروتونات في نواة ذرة ذلك العنصر، ويكتب أسفل رمز العنصر.
وإذا كانت الذرة متعادلة فإن:
العدد الذري = عدد البروتونات = عدد الإلكترونات
أما العدد الكتلي فيمثل مجموع البروتونات والنيوترونات في نواة ذرة العنصر، ويكتب أعلى رمز العنصر.
العدد الكتلي = عدد البروتونات + عدد النيوترونات
ويمكن حساب عدد النيوترونات من العلاقة:
عدد النيوترونات = العدد الكتلي - العدد الذري
مثال:
العدد الذري للأكسجين = 8 والعدد الكتلي = 16
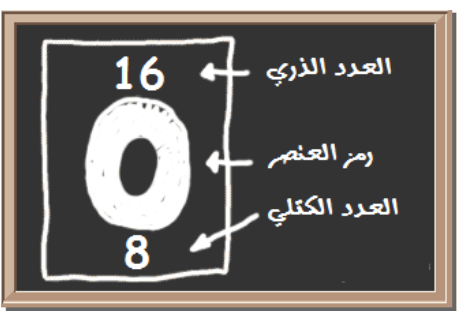
- عدد البروتونات = 8 (العدد الذري)
- عدد الإلكترونات = 8 (العدد الذري)
- عدد النيوترونات = 8 (العدد الكتلي – العدد الذري)
إعداد : شبكة منهاجي التعليمية
26 / 06 / 2025
النقاشات